 للأعلان
للأعلان 
رئيس قسم الزيوت والدهون بمعهد بحوث الصناعات الغذائية والتغذية بالمركز القومي للبحوث.
حين تختلط المصطلحات، تضطرب الأحكام. كم من نتيجة تحليل للزيوت أُسيء فهمها، وكم من تقديرٍ فني أو تجاري انحرف عن مساره، بسبب الخلط بين رقم الحامض، والـ % للحموضة، وقيمة الـ pH.
وللأسف، فإن هذا الالتباس لا يقع عند غير المتخصصين فحسب، بل يتسلل أحيانًا إلى بعض المعامل، ويتكرر لدى كثير من المتعاملين مع زيت الزيتون على امتداد سلسلة الإنتاج والتداول والتقييم. ذلك أن تشابه الألفاظ يوهم بالتقارب، بينما الحقيقة العلمية تقول غير ذلك؛ فلكل مصطلح مدلوله الخاص، ووحدته المستقلة، وطريقته في الحساب، ودلالته التحليلية التي لا يجوز الخلط بينها.
ومن هنا يأتي هذا المقال ليضع كل مفهوم في موضعه الصحيح، ويقدّم قراءة علمية واضحة تفك هذا الاشتباك الشائع، وتمنح المتلقي فهمًا أدق لنتائج تحليل الزيوت والدهون، ولا سيما زيت الزيتون، حيث تزداد الحاجة إلى الدقة، ويصبح ضبط المصطلح جزءًا من ضبط الحكم نفسه.
الخلاصة المباشرة:
رقم الحامض هو تعبير معايري عن عدد ملليجرامات هيدروكسيد البوتاسيوم (KOH) اللازمة لمعادلة الأحماض الدهنية الحرة الموجودة فى 1 جرام زيت أو دهن، ويُعبَّر عنه بوحدة mg KOH/g، بينما تمثل الحموضة ترجمةً لهذه النتيجة إلى نسبة مئوية محسوبة على أساس حمض مرجعي محدد، مثل حامض الأوليك أو البالميتيك أو اللاوريك؛ أما قيمة pH فليست مرادفًا لأيٍّ منهما، لأنها مقياس لنشاط أيونات الهيدروجين في الأوساط المائية، وليست مقياسًا لمحتوى الزيت من الأحماض الدهنية الحرة ولا تستخدم فى مجال الزيوت أساسا.
رقم الحامض هو عدد المليجرامات من هيدروكسيد البوتاسيوم KOH اللازمة لمعادلة الأحماض الدهنية الحرة الموجودة في 1 جم من الزيت أو الدهن. لذلك فهو يعبر عن شدة الحموضة المعايرية في العينة، ووحدته mg KOH/g.
ومن الناحية العملية فإن ارتفاع رقم الحامض يدل غالبا على زيادة التحلل المائي للدهون الثلاثية وتحرر الأحماض الدهنية الحرة، ولذلك يستخدم مؤشرا مهما على جودة الخامات وظروف التخزين والتداول.
الحموضة المئوية هي نفس نتيجة المعايرة، لكن بعد تحويلها إلى نسبة مئوية وزنية من حمض مرجعي واحد مفترض. ولهذا يجب دائما ذكر أساس التعبير: هل الحموضة محسوبة كحامض أوليك، أم بالميتيك، أم لاوريك؟
فإذا قيل إن الحموضة 1% دون بيان الحمض المرجعي، أصبحت العبارة ناقصة علميا؛ لأن القيمة العددية تتغير بتغير الكتلة المولية للحمض الذي نعبر به عن النتيجة.
السبب الحقيقي أن العلاقة بين رقم الحامض والحموضة % ليست علاقة ثابتة واحدة، بل تعتمد على الكتلة المولية للحمض المرجعي المختار للتعبير عن النتيجة. لذلك فالتقريب الشائع بأن الحموضة تساوي نصف رقم الحامض ينطبق فقط تقريبا عندما تكون الحموضة محسوبة كحامض أوليك.
Acid Value = (V x C x 56.1) / mAcidity % as X = (V x C x Mx) / (10 x m)Acidity % as X = Acid Value x (Mx / 561)إذا كان رقم الحامض = 4.00 mg KOH/g، فإن الحموضة تختلف باختلاف الحمض المرجعي كما يلي:

وهذا المثال وحده يثبت أن العينة نفسها يمكن أن تعطي أكثر من قيمة للحموضة % بحسب طريقة التعبير، بينما يظل رقم الحامض نفسه ثابتا لأنه هو النتيجة المعايرية الأصلية.
وبالمثل، إذا كانت الحموضة 1.00%، فإن رقم الحامض المقابل يساوي تقريبا 1.99 إذا كانت محسوبة كأوليك، و 2.19 إذا كانت محسوبة كبالميتيك، و 2.80 إذا كانت محسوبة كلاوريك.
في بعض الزيوت، وعلى رأسها زيت الزيتون، تُعبِّر المواصفات التجارية والتشريعية غالبًا عن الحموضة الحرة على أساس حامض الأوليك. لذلك فإن عبارة مثل 0.8% Acidity في زيت الزيتون لا تعني مطلقًا أن رقم الحامض (Acid Value) = 0.8، وإنما تعني أن الحموضة الحرة محسوبة كحامض أوليك، وهي قيمة تقابل تقريبًا 1.59 mg KOH/g كرقم حامض.
أما في زيوت ودهون أخرى، ولا سيما تلك التي يغلب في تركيبها نوع مختلف من الأحماض الدهنية، فقد يكون من الأدق أو من المتبع علميًا التعبير عن الحموضة على أساس حمض مرجعي آخر أكثر ملاءمة. ومن هنا تنشأ كثير من الأخطاء في قراءة تقارير التحليل أو تفسيرها، حين يُخلَط بين رقم الحامض (Acid Value) والحموضة المئوية (Acidity % / FFA%)، أو حين تُذكر الحموضة دون تحديد الحمض المرجعي الذي حُسبت على أساسه.
تنبيه مهم: حموضة الزيت ليست هي قيمة pH
ومن صور الالتباس الشائعة أيضًا الخلط بين حموضة الزيت والرقم الهيدروجيني (pH)، مع أن لكل منهما دلالة علمية مختلفة تمامًا. فقيمة pH هي مقياس لنشاط أيونات الهيدروجين في الأوساط المائية، ولذلك تُستخدم في توصيف محاليل وسوائل مثل العصائر والمحاليل المائية، ولا تُعد وصفًا قياسيًا مباشرًا لجودة الزيوت والدهون، لأن الزيت وسط غير مائي بطبيعته.
أما المقصود بـ "حموضة الزيت" في تقارير التحليل، فهو محتواه من الأحماض الدهنية الحرة الناتجة عن تحلل جزء من الجليسريدات، ويُعبَّر عنها إما في صورة النسبة المئوية للأحماض الدهنية الحرة (FFA / Acidity %) على أساس حمض مرجعي محدد، أو في صورة رقم الحامض (Acid Value) بوحدة mg KOH/g. ومن ثم، فإن استخدام pH بدلًا من هذه المؤشرات في وصف الزيوت يُعد خلطًا مفاهيميًا وتحليليًا ينبغي التنبه له.
رقم الحامض هو النتيجة المعايرية الأصلية بوحدة mg KOH/g، أما الحموضة % فهي ترجمة لهذه النتيجة إلى نسبة مئوية محسوبة على أساس حمض مرجعي محدد؛ ولذلك فهي ليست نصف رقم الحامض دائما، بل تكون قريبة من النصف فقط عندما تعبر كحامض أوليك.
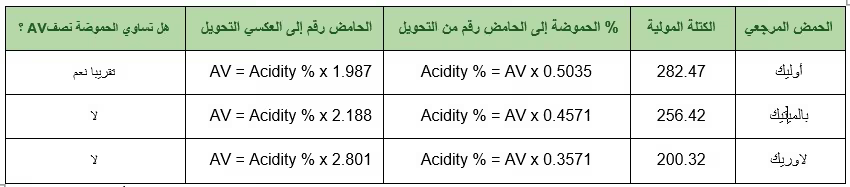
ملاحظة تفسيرية: شيوع عبارة "الحموضة تساوي نصف رقم الحامض" يرجع إلى التداول الواسع للتعبير بالحامض الأوليك، لكنه ليس قاعدة عامة لكل الزيوت والدهون ولا لكل طرق عرض النتائج.